
随着医疗器械不良事件的频发,世界各国都将医疗器械唯一标识UDI作为势在必行的举措。中国国家药监局在2021最新修订《医疗器械监督管理条例》中就明确指出“国家根据医疗器械产品类别,分步实施医疗器械唯一标识制度,实现医疗器械可追溯”。国家药监局规划医疗器械唯一标识覆盖全国所有医疗器械。第一批试点工作已经开展,但这只是开始,未来将进一步推动此项工作。这将表示UDI不仅仅是医疗器械产业打入国际市场的入门要求,也将会是医疗器械产品在国内市场的“身份证”。
UDI(即医疗器械唯一标识Unique Device Identification),它不仅仅是一串代码这么简单。它包含了医疗器械产品从医疗器械产品研发、生产、经营、使用的各个阶段信息。它实现了医疗器械产品的透明化、可视化,以及可追溯化,是医疗器械监管水平提升的重要手段。而要实现UDI的生成又将需要一整套系统融合而成。

博威Open PLM医疗器械唯一识别码UDI供应链追溯全生命周期管理系统是为了协助医疗器械企业管理UDI各阶段信息及UDI的生成所研发。整个系统管理范围涵盖产品从需求评估、产品研发设计项目立项与研发全过程、测试验证、试产及临床试验再到上市量产的全生命周期管理。系统功能模块包含有项目管理、产品数据管理、图文管理、工程变更管理、品质问题及规划等。
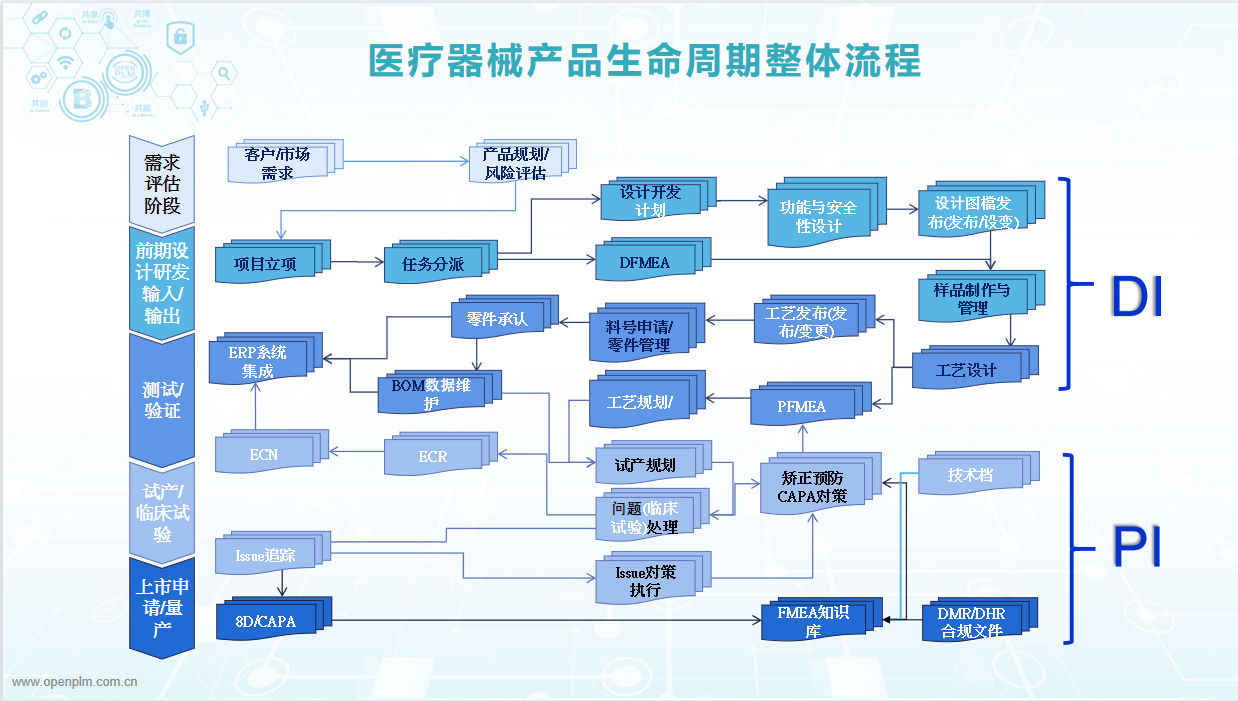
博威Open PLM医疗器械唯一识别码UDI供应链追溯全生命周期管理系统最终的目的是为了实现UDI唯一识别码的生成。UDI唯一识别码包含DI产品静态信息(企业编码、产品名称、包装等级、规格型号等)和PI产品动态信息(包括生产日期、失效日期、生产批次、序列号、校检位等)。
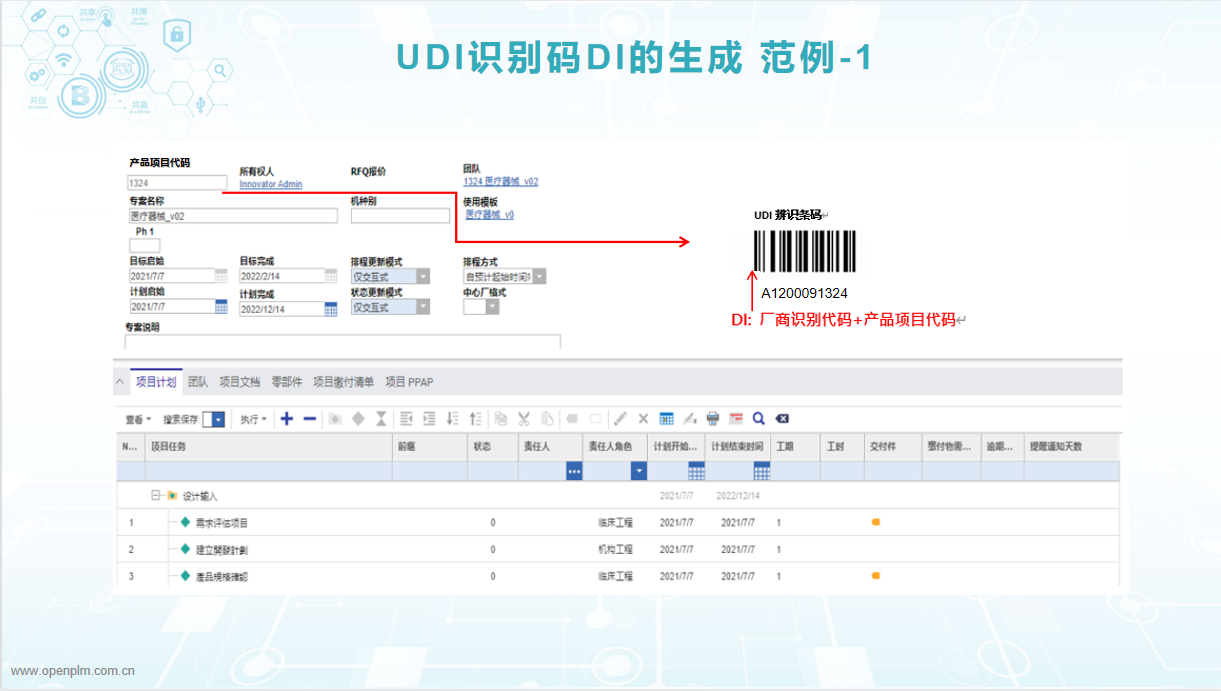
医疗器械UDI唯一识别码的广泛运用将势在必行,起到有效的市场监管的同时还能协助器械制造厂商达到以下目的:
>减少医疗差错;
>简化将器械使用信息集成到数据系统的操作;
>更加迅速地识别出现不良事件的医疗器械;
>更加迅速地为已报告的问题制定解决方案;
>提供更加迅速、更有效的器械召回解决方案;
>实现更加重点突出且有效的FDA安全沟通;
>轻松访问明确器械标识信息的原始来源。
而Open PLM医疗器械唯一识别码UDI供应链追溯全生命周期管理系统在实现以上目的的基础上能提供更规范化、智能化,便捷且有效的协助。
>提供标准化标识码,应用自动化识别技术的管理来取代人工作业
>透过UDI识别与数据库使用,可快速掌握院内器材库存状况与回报
>破除“信息孤岛”,联合供应链上下游业务一起推进应用UDI,实现医疗器械供应链的更全面的全程追溯(Full traceability system)。
为了帮助医疗器械行业内企业满足国家要求(2021年底前完成UDI唯一识别码与国家数据库的对接),博威团队在致众法规专家的指导之下, 初步实现数据库对接开发, 帮助企业能快速取得相应辨识编码并做好后续的产品开发及生产制造履历的追溯任务。双方就Open PLM医疗器械唯一识别码UDI供应链追溯全生命周期管理系统的推广达成了战略合作。
致众科技是一个以技术、人才为基础的团队,专注做医疗器械技术转化的服务。致众科技的近百名员工,有70多人与技术有关,专业集中在生物、光电和临床,而非大多数人想象的法律。他们以技术的眼光来研究医疗器械的合规问题,在创业者和监管部门之间成为一个沟通平台,更好地让技术来符合标准,帮助初创型企业在合规路上少走弯路。致众科技已帮忙包含华大基因、安翰科技、武汉博激、明德生物等众多光谷生物城明星企业在注册合规方面取得重要成果,为武汉杨森人工血管、杭州微泰胰岛素泵等高风险器械提供了有效的技术法规服务。
博威与致众一样,抱持工匠精神,希冀成为有产业价值的公司,能够真正帮助到产业的发展。本次双方在Open PLM医疗器械唯一识别码UDI供应链追溯全生命周期管理系统上通力合作,必将发挥多重效益,助力医疗器械产业在数字化管理领域转型升级,蓬勃发展。
请识别下方二维码,观看直播(Open PLM医疗器械唯一识别码UDI供应链追溯全生命周期管理系统说明及体验)

